Nobelpreis-Technologie im BOKU-VIBT Imaging Center
Das BOKU-VIBT Imaging Center wurde im Sommer 2010 am Vienna Institute of BioTechnologie (VIBT) am Standort Muthgasse der Universität für Bodenkultur Wien gegründet. Die Anlage war mit einer beeindruckenden Infrastruktur von fünf High-End-Forschungsmikroskopen ausgerüstet. Diese Infrastruktur wird stetig weiter entwickelt: die Einführung der neuesten Technologien steht immer im Fokus der Benutzer und Leitung der Anlage. Im Rahmen des durch das BMWFW kofinanzierte Hochschulraumstrukturmittel (HRSM)-Projekts "Ausbau von Synergien in Medizinischer Biotechnologie, Molekularer Zellbiologie und Zelltherapie" der BOKU, der Vetmeduni Wien und des "Institute for Science and Technology (IST) Austria" wurden vor kurzer Zeit zwei Mikroskope angeschafft: ein Lichtmikroskop kombiniert mit einem Raman-Spektrometer und ein Super-Auflösung-Mikroskop (gSTED).
Jahrhundertelang war die Entwicklung der Mikroskope von den Fähigkeiten der Linsenmacher abhängig. Eine feine Manufaktur, die wurde dann mit Feinmechanik und Elektronik gekoppelt. Nur ein einzelner Bestandteil der bildgebenden Systeme blieb unberührt: das Licht selbst, das die ultimative Auflösung eines Lichtmikroskops durch die Interaktion mit Objektiven zu diktieren schien.
Der deutsche Physiker, Stefan Walter Hell, der die Technologie der STED-Systeme erfunden und entwickelt hat, war einer der drei Wissenschaftler, die den Nobelpreis für Chemie in 2014 erhalten haben. Die Feinabstimmung und Kontrolle des Ein- und Ausschaltens von individuellen, fluoreszierenden Molekülen waren die geniale Neuerung seines Systems. Der Trick, der angewandt wurde, basiert auf einem bekannten Phänomen, das bereits Albert Einstein im Jahr 1917 prognostiziert hat. Mit intensiver Beleuchtung ist es möglich Atome bzw. Moleküle aus einem höheren, angeregten elektronischen Zustand zurück in den Grundzustand gehen zu lassen. Mit anderen Worten, mit Hilfe von Licht, kann man entweder in einem gut definierten Volumen (wie im Fall der STED Mikroskopen) oder zufällig in Raum und Zeit (superauflösende Bildaufnahme mit stochastischen Methoden wie STORM, PALM) Fluorophore ein- und auszuschalten.
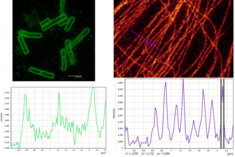
In Abhängigkeit von der Super-Auflösungstechnik kann die vorgesehene Auflösung vier- bis zehnmal besser sein als bei herkömmlichen Fluoreszenz-Mikroskopen, also auch 20 nm Auflösung ist erreichbar. Somit macht die Super-Auflösung Mikroskopie sogar Viren sichtbar. Obwohl Elektronenmikroskopie noch eine bessere räumliche Auflösung bietet, ist damit ein erheblicher Nachteil verbunden: Elektronenmikroskopie kann nur mit wasserfreien Proben arbeiten. Sie erlaubt es nicht, feine Strukturen zu untersuchen, wenn die Probe lebt bzw. sich bewegt. Super-Resolution Mikroskopie kann das tun: ein STED-Mikroskop ermöglicht die Visualisierung zierlicher Details auch in lebenden Proben.
Das erste STED-System in Wien wurde an der BOKU-VIBT Imaging Center installiert und steht für die gesamte wissenschaftliche Gemeinschaft der Hauptstadt zur Verfügung. ForscherInnen, die unser gSTED-System nutzen möchten, sind willkommen und sollen sich diesbezüglich an Dr. Monika Debreczeny (monika.debreczeny(at)boku.ac.at) wenden.