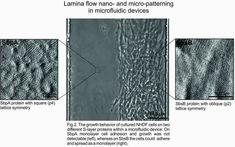
Lebende Zellen sind sehr empfindlich gegenüber topographischen als auch chemischen Veränderungen innerhalb der extrazellulären Matrix (ECM). Die Fähigkeit, Flächen technisch herzustellen, die die ECM-Komponenten imitieren, die Adhäsion und das Ausbreiten und das Wachstum von Zellen auf nanostrukturierten Oberflächen kontrollieren ist ein kritischer Faktor für die Herstellung von medizinischen Implantaten und für funktionelle Gerüste bestehend aus Biomaterialien für das Tissue Engineering, sowie für die Entwicklung von Zell-integrierenden Biochips als zellbasierte Sensoren und Lab-on-a-Chip bioanalytische Geräte. S-Schichtproteine sind gut untersucht Selbstorganisationssysteme. Die in-vitro Rekristallisationseigenschaften von nativen und gentechnisch veränderten S-Schichtproteinen, die zweidimensionale Gitterstrukturen in Suspension, auf festen Trägern und Phasengrenzflächen bilden, ermöglichen deren Anwendung für die Oberflächenstrukturierung. Aufgrund ihrer strukturellen und funktionellen Vielfalt zeigen monomolekulare S-Schichten völlig unterschiedliche Oberflächeneigenschaften im Hinblick auf die Zelladhäsion und Ausbreitung von humanen Primärzellen und Tumorzelllinien. Wie in Abbildung 2 für NHDF-Zellen gezeigt, stellt die S-Schicht bestehend aus SbsB Proteinen eine biokompatible Oberfläche für das Zellwachstums bereit während die S-Schicht bestehend aus SbpA Proteinen als Anti-Fouling Oberfläche wirkt und somit keine Zellhaftung und Wachstum auftritt. Daher ermöglichen S-Schichten die Entwicklung von vielversprechenden Strategien für die Herstellung von Zellmustern auf verschiedenen Substraten und das Design neuer Biomaterialien. Kontaktperson: Ass.Prof.Dipl.-Ing. Dr.tech Seta Küpcü